Venus Concept anuncia la autorización FDA 510(K) para Venus Viva MD
Venus Viva MD permite un amplio espectro de tratamientos en la consulta del médico estético y el dermatólogo para la estética
-
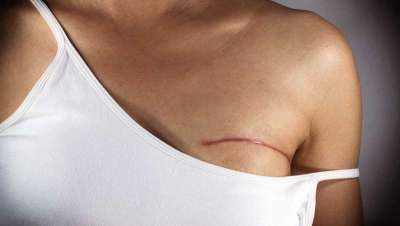
Avanzar con el paciente oncológico
-
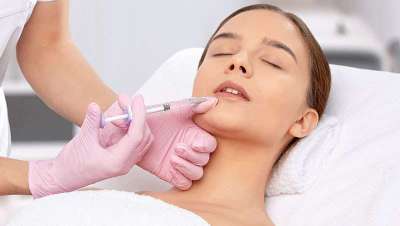
Un total de 18 millones de intervenciones de cirugía estética en Estados Unidos
Con un despunte claro de las intervenciones de cirugía estética corporales, los métodos faciales mínimamente invasivos sin embargo también aumentan en una tendencia clara de aumento del consumo a nivel mundial
-
Ultherapy Prime® redefine la firmeza corporal: nueva indicación para brazos y abdomen
La tecnología de ultrasonidos microfocalizados avanza hacia tratamientos corporales más precisos, personalizados y no invasivos.
-
Cellfina, el tratamiento definitivo contra la celulitis
Cellfina, de Merz Aesthetics, es el único procedimiento mínimamente invasivo aprobado por la UE para tratar los hoyuelos y la piel de naranja característicos de la celulitis. Ahora aterriza desde EE UU al Centro de Dermatología Pedro Jaén
-
La tecnología que estimula el colágeno desde el interior
La forma de tratar la flacidez sin cirugía pasa por un procedimiento no invasivo que redefine el rostro y mejora la firmeza de manera progresiva.
-
Antioxidantes mitocondriales: el futuro de la longevidad de la piel
Un nuevo enfoque cosmético protege las células desde el interior y combate los signos visibles del envejecimiento
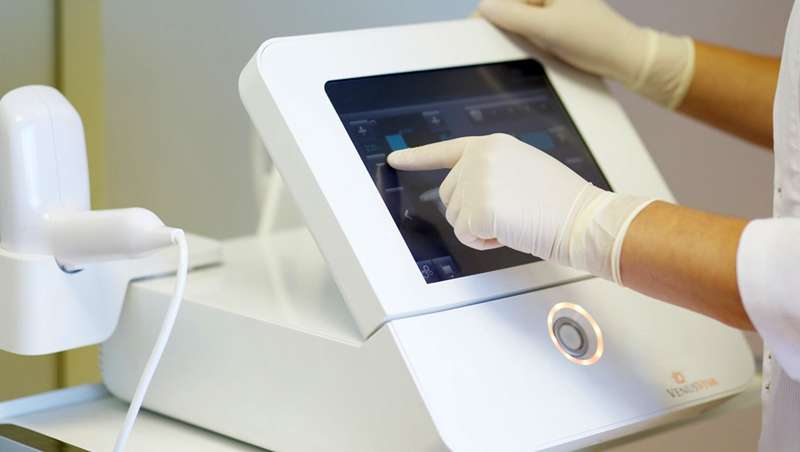
Venus Concept Inc. ha hecho público que ha recibido la autorización FDA 510(k) para comercializar y vender Venus Viva MD.
Venus Viva MD es un dispositivo no invasivo destinado a ser utilizado por médicos o dermatólogos relacionados con la estética. Un equipo de sobremesa portátil y versátil que permite una amplia gama de tratamientos con dos aplicadores.
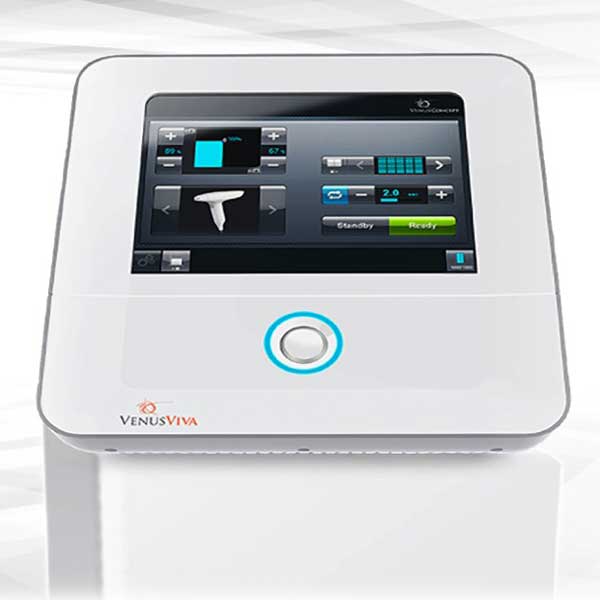
Cuando se utiliza con el nuevo aplicador Viva MD, el dispositivo Venus Viva MD está diseñado para su uso en procedimientos dermatológicos que requieren ablación y rejuvenecimiento de la piel, incluyendo condiciones tales como cicatrices de acné, discromia, estrías y poros agrandados. "Nos complace anunciar la autorización FDA 510(k) para nuestro dispositivo Venus Viva MD y nos estamos preparando para comenzar un lanzamiento limitado al final del tercer trimestre", dice Domenic Serafino, CEO y director del concepto Venus.
"El Venus Viva MD es un producto que diseñamos específicamente para dermatólogos y cirujanos plásticos en los Estados Unidos, que aprovecha nuestras sólidas ofertas de rejuvenecimiento de la piel en Venus Viva y Venus Versa, pero ofrece características diferenciadas que permiten a los médicos de la comunidad de estética médica tradicional tratar una gama más amplia de condiciones de la piel. Es importante destacar que esta nueva introducción de productos es otro ejemplo de nuestro continuo enfoque en la introducción de soluciones tecnológicas nuevas e innovadoras cada año, al tiempo que identificamos formas de mejorar las contribuciones a nuestro crecimiento general de la venta de piezas de mano basadas en la utilización a lo largo del tiempo. Esperamos que la comercialización estadounidense del Venus Viva MD contribuya al perfil de crecimiento a largo plazo de la compañía y creemos que nuestra amplia cartera de soluciones de rejuvenecimiento de la piel nos ayudará a penetrar aún más en el mercado mundial de dispositivos estéticos basados en energía de 3.400 millones de dólares en los años venideros".

Recomendamos