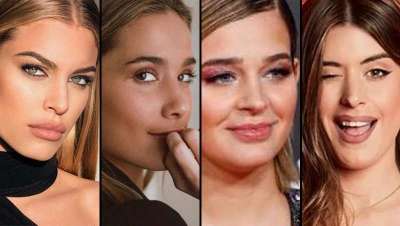RMD 2017, cuenta atrás para su segunda edición
El Simposio Europeo sobre el Nuevo Reglamento Acordado de Dispositivos MĂ©dicos (RMD2017) prepara su prĂłxima ediciĂłn en el Hotel Hilton de BerlĂn (Alemania), del 16 al 17 de octubre de 2017
-
Antioxidantes mitocondriales: Âżmoda o evoluciĂłn real?
-
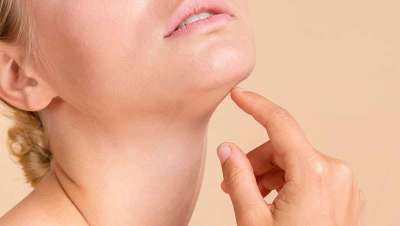
Cellfina, el tratamiento definitivo contra la celulitis
Cellfina, de Merz Aesthetics, es el Ăşnico procedimiento mĂnimamente invasivo aprobado por la UE para tratar los hoyuelos y la piel de naranja caracterĂsticos de la celulitis. Ahora aterriza desde EE UU al Centro de DermatologĂa Pedro JaĂ©n
-
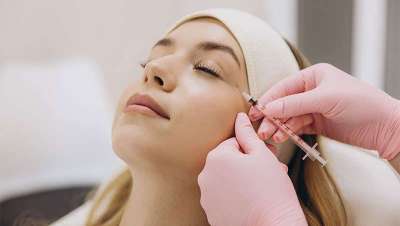
Veinteañeras y neuromoduladores: ¿presión o expresión?
QuerĂamos entender a fondo este fenĂłmeno tan desconcertante. Para ello, hemos hablado con la doctora Marta Garay, mĂ©dica especialista en medicina estĂ©tica facial y corporal del Grupo Pedro JaĂ©n. Esto es lo que nos contĂł
-
MarĂa Pombo, Jessica Goicoecha, Laura Escanes y Dulceida, los retoques estĂ©ticos de las influencers
Hoy, cuatro de nuestras socialitĂ©s más famosas nos descubren sus principales retoques estĂ©ticos y cĂłmo estos han cambiado su fisionomĂa... ¡a mejor!, por supuesto
-
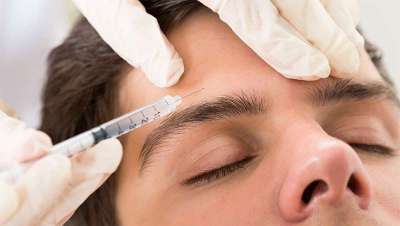
Del 'brotox' a la mandĂbula de diamante: 5 tratamientos que impulsan la estĂ©tica masculina
El auge de los tratamientos médicoestéticos entre los hombres se consolida a nivel mundial, impulsado por una mayor información del paciente y por procedimientos cada vez más naturales y personalizados
-
Qué es la edad biológica y por qué es importante
La edad biológica revela cómo envejecen realmente nuestras células y se convierte en la clave para anticipar salud, enfermedad y calidad de vida, tal como explica Longevytum
Tras el éxito del congreso inaugural en Praga, la segunda edición del Simposio Europeo sobre el Nuevo Reglamento Acordado de Dispositivos Médicos (RMD) abordará las principales actualizaciones de los dispositivos médicos.
En conjunción con la EAAR (Asociación Europea de Representantes Autorizados), una importante delegación de profesionales con gran experiencia en este campo, volverá a garantizar un simposio de calidad notable.

Los temas a cubrir serán, entre otros:
- Nuevas normas que refuerzan las leyes sobre la comercializaciĂłn de productos sanitarios.
- Vigilancia de refuerzo.
- Responsabilidades de los fabricantes para el control de la calidad, el rendimiento y la seguridad de sus dispositivos.
- La mejora de la trazabilidad en toda la cadena de suministro.
- La actualizaciĂłn de la base central de datos para ofrecer a los pacientes, a los profesionales de la salud y al pĂşblico informaciĂłn completa sobre los productos disponibles en el mercado de la UE.
- Representante autorizado versus Persona cualificada.
Todos estos temas se actualizarán una vez finalizado el orden del dĂa.

Recomendamos