Más allá de la barrera cutánea: el papel de la inflamación tipo 2 en la dermatitis atópica a través de las edades
Reproducimos lo más destacado del simposio patrocinado por Sanofi y Regeneron Pharmaceuticals durante el congreso de la Academia Europea de Dermatología 2022
-
Avanzar con el paciente oncológico
-
Maribel Yébenes apuesta por la longevidad y la medicina estética integrativa con la incorporación de la Dra. Karen Wejbe
Una nueva visión donde la precisión clínica, la regeneración y el enfoque a largo plazo redefinen la sofisticación estética.
-
Sesderma lanza el contorno de ojos y labios de la gama exoses
La línea pionera con exosomas incorpora un nuevo cuidado específico para las zonas más delicadas del rostro.
-
Ferraro, la nueva clínica de medicina estética que democratiza los cuidados y tratamientos estéticos
Espacio que combina la tecnología más avanzada en medicina-estética del sector con los rituales de Alqvimia ancestral. El Dr. Tomás Zamora dirige al equipo de la clínica que apuesta por un enfoque único y exclusivo con resultados reales y duraderos
-
En qué consiste el countouring estético
Un óvalo facial firme, con un aspecto terso y joven es posible gracias a inyectables con activos quemagrasa realmente efectivos
-
Ultherapy Prime® redefine la firmeza corporal: nueva indicación para brazos y abdomen
La tecnología de ultrasonidos microfocalizados avanza hacia tratamientos corporales más precisos, personalizados y no invasivos.
La dermatitis atópica (EA) pediátrica es común. El estudio EPI-CARE (discutido a continuación), por ejemplo, informó que el 12.1% de los niños de entre 6 meses y 5 años en 18 países tenían EA. La prevalencia de EA fue similar en todos los grupos de edad: 13,0% de las personas de 6 a 11 años y 14,8% de las personas de 12 a 17 años.1 La EA, especialmente cuando es moderada o grave, puede tener un impacto perjudicial en la vida del niño y en las actividades de la familia.2,3 Sin embargo, muchos niños elegibles con EA moderada a grave no reciben terapias sistémicas y todavía tienen una enfermedad no controlada, medida por la frecuencia y la duración de los brotes.4
En este contexto, el simposio educativo (patrocinado por Sanofi y Regeneron Pharmaceuticals) celebrado durante el congreso de la Academia Europea de Dermatología y Venereología (EADV) de 2022, revisó la carga de la EA en los niños y sus cuidadores. El simposio también consideró los desarrollos recientes en el tratamiento de la EA pediátrica moderada a grave.5,7
Otro segundo simposio educativo durante el congreso EADV 2022 exploró la interrelación entre la inflamación tipo 2, la disfunción de la barrera cutánea y la desregulación neuroinmune en la EA. La inflamación tipo 2 involucra varias células (por ejemplo, linfocitos T-helper 2 [Th2], eosinófilos, mastocitos, basófilos y células linfoides innatas tipo 2) y varias citoquinas (por ejemplo, IL-4, IL-13 e IL-5).8 Los oradores revisaron las vías a través de las cuales la inflamación tipo 2 socava la integridad de la barrera cutánea y promueve la neuroinflamación. Esta tríada de disfunción tipifica y contribuye a la EA.
La carga de la EA en los niños y sus cuidadores
El profesor Paolo Amerio, Clínica de Dermatología, Departamento de Medicina y Ciencias del Envejecimiento, Universidad D'Annunzio Chieti-Pescara, Chieti, Italia, revisó la evidencia de que la EA pediátrica dificulta muchos aspectos del funcionamiento diario del niño. Los niños con EA de moderada a grave, generalmente experimentan brotes e infecciones de la piel frecuentes y duraderos, problemas para dormir y somnolencia diurna. La EA pediátrica también puede tener consecuencias negativas a largo plazo en el curso de la vida del niño que surgen, por ejemplo, del impacto en la escolarización, la estigmatización social y las relaciones.1,9
El profesor Amerio señaló que, hasta hace poco, muchos estudios que evaluaban la carga impuesta por la EA se centraban en un solo centro, eran transversales en lugar de longitudinales y no se estratificaban según la gravedad de la enfermedad. Un análisis de subgrupos de la encuesta en línea EPI-CARE, que incluyó a 517 niños de 6 meses a 6 años de Europa, abordó estas limitaciones.6
La carga sobre los pacientes y cuidadores aumenta a medida que la EA se vuelve más grave
La mayoría de los niños en EPI-CARE tenían EA leve. La proporción de niños que experimentaron más de dos brotes en el último mes aumentó del 4,9% de aquellos con EA leve al 22,3% y 46,9% en niños con EA moderada y grave, respectivamente.6
La proporción en la que la duración media del brote duró al menos 2 semanas aumentó del 9,0% de aquellos con EA leve al 24,5% y 49,2% en niños con EA moderada y grave, respectivamente.6
Otro estudio, que revisó los registros médicos del Reino Unido, encontró que los niños con EA de inicio temprano (≤7 años) tenían más probabilidades de desarrollar infecciones de la piel que aquellos con EA de inicio tardío (inicio entre 8 y 17 años).10 Después de ajustar por edad, sexo, duración del seguimiento y otras comorbilidades atópicas, aquellos con EA de inicio tardío tenían entre un 19% y un 26% menos de probabilidades de tener molusco contagioso (odds ratio [OR] 0.74), varicela o herpes zóster (OR 0.75), impétigo (OR 0.78) y herpes simple (OR 0.81) que aquellos con inicio de EA a los ≤7 años. Los niños con EA de inicio tardío tenían aproximadamente un 10% menos de probabilidades de tener celulitis (OR 0.90) y verrugas (OR 0.91) que aquellos con una edad de inicio más temprana.10
Comorbilidades atópicas
La mayoría de los niños con EA tienen al menos una comorbilidad atópica. La encuesta en línea PEDIBURDEN incluyó a 160 niños de 6 a 11 años con EA moderada y grave. Las comorbilidades atópicas comunes incluyeron: alergia al polen (52,5%); alergia al polvo o a los ácaros (46,3%); conjuntivitis alérgica (35,0%) y alergia alimentaria (33,1%).11 El profesor Amerio señaló que las comorbilidades atópicas empeoraron varios resultados relacionados con la EA, incluida la privación del sueño, en comparación con los niños con EA sola.
La encuesta PEDI-BURDEN también informó que aproximadamente la mitad de los niños con EA y aproximadamente la misma proporción de sus cuidadores habían dormido mal en la última semana.7 Además:
- Los niños con EA informaron una media de 91,7 noches inquietas al año en comparación con 8,5 noches entre los niños sin EA.9
- Los niños con EA informaron sentirse somnolientos en una media de 63,1 días al año en comparación con 6,5 días entre los niños sin EA.9
- Los cuidadores de niños con EA informaron trastornos del sueño en una media de 86,7 noches al año en comparación con 23,3 noches entre los padres de niños sin EA.9
- Los cuidadores se sintieron somnolientos en una media de 97,8 días al año en comparación con 25,8 días entre los padres de control.9
Como sugieren los patrones de sueño de los cuidadores, la EA infantil afecta a toda la familia. La investigación del Estudio Pediátrico en Dermatitis Atópica (PEDISTAD) es un estudio longitudinal multinacional, basado en registros, en curso de niños menores de 12 años con EA moderada a grave que reciben medicamentos sistémicos para la EA, fototerapia o tratamientos tópicos, pero eran candidatos para la terapia sistémica. Según el Cuestionario de Impacto Familiar sobre Dermatitis (DFIQ), la EA afectó "bastante" o "mucho" a varias áreas de la vida familiar, incluidos los gastos (seleccionados por el 46,7% de los encuestados), el cansancio / agotamiento (40,7%), el sueño familiar (40,7%), la vida del cuidador debido al tratamiento de la EA (38,3%), la angustia emocional (37,5%), las tareas domésticas (32,6%), el ocio familiar (25,9%), la preparación / alimentación de alimentos (23,3%) y las relaciones familiares (18,4%).12
Evaluación del impacto
El profesor Amerio señaló que varias herramientas capturan varios aspectos de la "experiencia vivida" de las personas con EA, que incluyen:
- El área de eccema y el índice de gravedad (EASI) para los signos de EA.13
- La medida del eccema orientado al paciente (POEM) para los síntomas.14
- El Índice de Calidad de Vida de Dermatología Infantil (CDLQI)15 y el Índice de Calidad de Vida de la Dermatitis Infantil (IDQOL)16 para la calidad de vida (CdV) relacionada con la salud.
- Recapitulación del eccema atópico (RECAP) para el control de la enfermedad a largo plazo.17
Juntas, estas herramientas pueden construir una visión holística del impacto de la EA en los pacientes. Sin embargo, es posible que los médicos no tengan tiempo para implementar estas medidas en una práctica ocupada. Como mínimo, el profesor Amerio abogó por cuantificar la picazón utilizando preguntas verbales simples, como "En los últimos 7 días, ¿cuál fue la peor y la picazón promedio en una escala de 1 a 10?". Como señaló el profesor Amerio, la picazón es el síntoma más angustiante de la EA, que se correlaciona con la angustia mental y la falta de sueño.
Tratamiento actual de niños con EA de moderada a grave en todo el mundo
Dado el impacto en los pacientes, las familias y los cuidadores, los niños con EA moderada a grave necesitan tratamientos sistémicos bien tolerados y eficaces, comentó la profesora Anna Belloni Fortina, Jefa de la Unidad de Dermatología Pediátrica del Departamento de Medicina de la Universidad de Padua, Italia.
Sin embargo, la evidencia del mundo real demuestra que muchos niños elegibles con EA de moderada a grave no reciben terapia sistémica.4 PEDISTAD, por ejemplo, informó que solo el 31,6% de los niños menores de 12 años que se consideran candidatos para recibir tratamiento sistémico recibieron medicamentos sistémicos para la EA, más comúnmente dupilumab (12,0%), corticosteroides sistémicos (10,2%), ciclosporina (9,3%) y metotrexato (8,7%).4
Actualmente, sin embargo, hay pocos datos longitudinales sólidos a largo plazo que evalúen los resultados en niños con EA moderada a grave inadecuadamente controlada.30 PEDISTAD está recopilando datos sobre las características y la progresión de los pacientes y la enfermedad, las comorbilidades atópicas seleccionadas, los patrones de tratamiento en el mundo real, la eficacia y la seguridad durante 5 años.29,30
Al inicio del estudio, la EA afectó a una media del 33,3% (desviación estándar [DE] 21,0%) del área de superficie corporal (ASC). La puntuación media de EASI fue de 14,4 (DE 10,7) y la puntuación media de POEM fue de 15,6 (DE 7,2). Muchos niños con EA experimentaron picazón (65,0% experimentaron este síntoma todos los días), con piel seca / áspera (62,0%), agrietada (40,7%) y descamación (39,2%), y AD afectó el sueño (31,6%).29
Resultados sistémicos del tratamiento
El profesor Belloni Fortina presentó los resultados provisionales de PEDISTAD después de 2 años de seguimiento en tres cohortes de pacientes tratados con dupilumab (n = 144), metotrexato (n = 114) y ciclosporina (n = 121) La puntuación total de EASI mejoró en: 31
58,9% en comparación con el valor basal después de una mediana del período de observación del tratamiento de 8,1 meses 20,9 a 8,6) con dupilumab (p<0,001).
33,7% después de una mediana de observación del tratamiento de 13,0 meses con metotrexato (16,6 a 1,0; p<0,001). La ciclosporina no se asoció con una diferencia estadísticamente significativa en la puntuación total de EASI después de una mediana del período de observación del tratamiento de 10,7 meses (18,8 a 15,5).
Los tres tratamientos, sin embargo, redujeron la BSA afectada:31
Dupilumab se asoció con una mejoría del 50,0% en la BSA afectada, disminuyendo del 39,8% al inicio del estudio al 19,9% (p<0,0001).
El metotrexato se asoció con una mejoría del 34,8% en los afectados por BSA (33,9% al inicio del estudio a 2,21%; p<0,0001).
La ciclosporina se asoció con una mejoría del 21,7% en los afectados por BSA (40,6% al inicio del estudio hasta 31,8%; p<0,001).
Dupilumab y metotrexato también mejoraron los síntomas de la EA reportados por los pacientes. La puntuación total media de POEM mejoró en un 38,5% (18,2 al inicio; 11,2 después de 8,1 meses; p<0,0001) con dupilumab y en un 26,7% con metotrexato (17,6 al inicio; 12,9 después de 13,0 meses; p<0,0001). La ciclosporina no se asoció con una diferencia estadísticamente significativa en la puntuación total de POEM (17,5 al inicio del estudio; 16,0 después de 10,7 meses).31
La incidencia de eventos adversos basada en datos preliminares después de 2 años de seguimiento fue del 18,1% con dupilumab, del 28,9% con metotrexato y del 31,4% con ciclosporina, respectivamente.31
El profesor Belloni Fortina señaló que la mayoría de los niños inscritos en el estudio PEDISTAD no recibían terapia sistémica y estaban mal controlados con terapia tópica.4 Por lo tanto, existe una importante necesidad médica de tratamientos sistémicos seguros y eficaces para la EA pediátrica moderada a grave.
Terapia sistémica dirigida para niños con EA: de los estudios clínicos a la práctica en el mundo real
El profesor Michael Cork, de la Universidad de Sheffield, Hospital de Niños de Sheffield, Reino Unido, señaló que los inmunosupresores sistémicos tradicionales no están aprobados actualmente para niños menores de 16 años y están asociados con efectos secundarios. Por ejemplo, la ciclosporina, utilizada para controlar los brotes agudos de la EA, puede aumentar la creatinina sérica y la presión arterial.32 El metotrexato y la azatioprina se usan como terapia de mantenimiento a largo plazo para las personas con EA, pero pueden causar efectos secundarios hematológicos y gastrointestinales, así como aumentos en los niveles de enzimas hepáticas.32
Debido a los problemas de tolerabilidad, los inmunosupresores sistémicos tradicionales requieren un control de seguridad regular. Por ejemplo, el monitoreo de ciclosporina y metotrexato incluye, entre otras pruebas, recuentos sanguíneos completos y diferenciales, detección de tuberculosis, función renal y hepática y, si está indicado, pruebas de VIH.32 Un estudio de fase III, parte del programa LIBERTY que se analiza a continuación, inscribió a 367 niños de 6 a 11 años con EA grave. El tratamiento con niños con EA moderada a grave fue sostenido dupilumab más corticosteroides tópicos (TCS) no se asoció con cambios clínicamente significativos en los parámetros de laboratorio para hematología, química sérica o análisis de orina.33
El programa LIBERTY
El profesor Cork resumió los resultados del programa LIBERTY, que inscribió a niños de 6 a 11 años.34,35 LIBERTY AD PEDS aleatorizó a 367 niños con EA grave a placebo, dupilumab subcutáneo 300 mg cada 4 semanas o dupilumab subcutáneo cada 2 semanas (<30 kg: 100 mg; ≥30 kg: 200 mg) durante 16 semanas. Todos los niños también recibieron TCS.34
LIBERTY AD PED OLE es un estudio de extensión abierta (OLE) en curso durante el cual 362 niños de LIBERTY AD PEDS o un estudio de fase II de 12 semanas de monoterapia con dupilumab recibieron dupilumab subcutáneo 2 mg/kg o 4 mg/kg semanalmente hasta que se dispusiera de datos farmacocinéticos y luego 300 mg cada 4 semanas. Los médicos pueden aumentar la dosis a 200 mg cada 2 semanas si <60 kg o 300 mg cada 2 semanas si ≥60 kg y pueden prescribir TCS concomitante con o sin inhibidor tópico de calcineurina. Los niños fueron seguidos por hasta 52 semanas. El objetivo de la OLE fue informar el perfil farmacocinético y la seguridad y eficacia a largo plazo de dupilumab en niños (de ≥ a 6 <12 años) con EA grave.35
Dupilumab mejoró significativamente las tasas de respuesta de EASI-75 en la semana 16, que se mantuvo durante las 52 semanas de seguimiento. En niños con EA grave, placebo más TCS produjo una tasa de respuesta EASI-75 del 27%. Dependiendo del régimen, dupilumab produjo tasas de respuesta EASI-75 de 67% y 70% (ambos p<0,0001).34 La mejoría en niños con EA moderada a grave se mantuvo: en la semana 52, el 79,4% mostró una respuesta EASI-75.35
LIBERTY AD PEDS y LIBERTY AD PED OLE utilizaron la escala analógica visual SCORing Atopic Dermatitis (SCORAD) (rango 0-10) para evaluar la picazón. En LIBERTY AD PEDS, las puntuaciones de picazón en niños de 6 a 11 años tratados con placebo más TCS disminuyeron de una media de 7,4 al inicio del estudio a 5,0 en la semana 16 (no significativa). Las puntuaciones en aquellos que recibieron dupilumab 300 mg más TCS disminuyeron de 7,8 al inicio del estudio a 2,6 en la semana 16 (p<0,001).36 Al ingresar al OLE, la puntuación media del prurito fue de 3,8. La puntuación continuó mejorando, alcanzando una media de 1,5 en la semana 52. En general, dupilumab redujo la gravedad del prurito de grave (puntuaciones de 7 a <9) a leve (0 a <4).36 El profesor Cork notó que la mejoría en la picazón asociada con dupilumab comenzó a surgir después de la primera inyección.
En un análisis post-hoc, dupilumab produjo mejoras sostenidas en la puntuación total de SCORAD durante las 52 semanas de seguimiento. La puntuación SCORAD total oscila entre 0 y 103. Las puntuaciones totales de SCORAD en niños tratados con placebo más TCS disminuyeron de una media de 72,9 al inicio a 51,1 en la semana 16 (no significativa). Las puntuaciones en aquellos que recibieron dupilumab 300 mg más TCS disminuyeron de 75.6 al inicio del estudio a 27.3 en la semana 16 (p<0.001).36 Al ingresar al OLE, la puntuación media de SCORAD fue de 35,5, que disminuyó a 18,8 en la semana 52 (no significativa). En general, dupilumab redujo la gravedad de la EA de grave (puntuaciones de >50) a leve (0-25) en la semana 16 (p<0,001).36
Mejoras en la calidad de vida
Dupilumab se asoció con mejoras significativas en la CdV para los niños con EA grave.37,38 En los niños tratados con placebo más TCS, el 35,8% de los ≥30 kg y el 48,3% de los <30 kg mostraron al menos una mejoría de seis puntos en la puntuación CDLQI en la semana 16, lo que sugiere una mejoría significativa en la CdV. Ninguna de estas mejorías con placebo más TCS fue estadísticamente significativa en comparación con el valor inicial. En la semana 16, el 81,8% de los que recibieron dupilumab 300 mg cada 4 semanas más TCS (p<0,001) y el 80,8% de los que recibieron dupilumab 200 mg cada 2 semanas más TCS (p<0,0001) mostraron al menos una mejoría de seis puntos en la puntuación CDLQI.37,38 Dupilumab también dio lugar a mejoras significativas en la CV para las familias de niños con EA grave. Para las familias de niños <30 kg que recibieron dupilumab 300 mg cada 4 semanas más TCS, el 73,4% informó una reducción en la carga familiar de la EA, que se evaluó mediante el DFIQ, en comparación con el 38,7% del grupo placebo más TCS. Una proporción similar (75,4%) de las familias de niños ≥30 kg que recibieron dupilumab 200 mg cada 2 semanas más TCS informaron una mejoría en comparación con el 40,6% del grupo de placebo más TCS.37
Eventos adversos
Dupilumab fue bien tolerado durante 16 semanas. El número de eventos adversos emergentes del tratamiento que condujeron a la interrupción fue similar en los grupos placebo más TCS (1,7%) y dupilumab 300 mg cada 4 semanas más TCS (0%) y 100 o 200 mg cada 4 semanas más TCS (1,6%). Las infecciones cutáneas fueron numéricamente más frecuentes con placebo (13,3%) que con cualquiera de los grupos de dupilumab (300 mg: 5,8%; 100 o 200 mg: 8,2%).34 La conjuntivitis (300 mg: 6,7%; 100 o 200 mg: 14,8%) y las reacciones en el lugar de la inyección (300 mg: 10,0%; 100 o 200 mg: 10,7%) fueron numéricamente más frecuentes con dupilumab que con placebo (4,2% y 5,8%, respectivamente). El profesor Cork señaló que la conjuntivitis era predominantemente ojo seco y, en su práctica clínica, la participación temprana de un oftalmólogo permite la implementación de medidas de mejora. El perfil de seguridad fue consistente con otros grupos de edad estudiados. No se observaron nuevas señales de seguridad en niños con EA en comparación con las observadas en adultos a las 16 semanas.34
El profesor Cork concluyó que las terapias dirigidas avanzadas pueden proporcionar mejores oportunidades de manejo para los niños con EA moderada a grave que los inmunosupresores sistémicos actuales.4,34-36,38
Relevancia de la señalización de tipo 2 en la EA
La inflamación tipo 2 parece haber evolucionado como una respuesta inmune especializada para promover la inmunidad de barrera en las superficies mucosas, en particular para eliminar helmintos (por ejemplo, gusanos redondos) y para apoyar la reparación de tejidos y la expulsión de gusanos.8,39 La creciente evidencia muestra que la inflamación tipo 2 es uno de los mediadores clave de la disfunción de la barrera y la neuroinflamación, que son características de la fisiopatología de la EA.
El profesor Donald Leung, Jefe de la División de Alergia e Inmunología Pediátrica, National Jewish Health en Denver, Colorado, EE.UU., ha estudiado la inflamación tipo 2 en la EA durante más de 30 años. Señaló que en las personas con EA, la inflamación tipo 2 interrumpe la función y la integridad de la barrera cutánea, aumenta la permeabilidad y promueve la disbiosis (el desequilibrio de la flora cutánea normal).40 La inflamación tipo 2 también resulta en estimulación neuronal, que en concierto con los cambios en la función de barrera de la piel, impulsa el ciclo crónico de picazón / rascado.40
Picazón e inflamación tipo 2.
El profesor Leung revisó la evidencia de que la picazón (prurito) es un componente central de la inflamación tipo 2.41 La respuesta de picazón puede haberse desarrollado para alertar a los pacientes que están infestados y la respuesta de rascado para eliminar los parásitos de la superficie de la piel.41 El rascado desencadena la proliferación de queratinocitos y fibroblastos, lo que promueve la reparación de heridas y puede "aislar" los parásitos restantes.41-46
La inflamación tipo 2 es la vía inflamatoria predominante en los subtipos de EA.47-52 Por ejemplo, las poblaciones de linfocitos Th2 y Th22 están marcadamente elevadas en europeos americanos, asiáticos, afroamericanos y niños con EA.47-52 También hay algunas diferencias. Por ejemplo, las células Th1 parecen aumentar en los estadounidenses de origen europeo y asiáticos con EA, pero no en los afroamericanos ni en los niños.47-52 El profesor Leung señaló que todavía hay mucho que aprender sobre la inflamación tipo 2.
IL-4 e IL-13 son mediadores distintivos de la inflamación tipo 2 y tienen múltiples funciones superpuestas en la EA.40-53 IL-4 e IL-13 median la inflamación y la disfunción de la barrera a través de cambios inmunológicos y estructurales, mejoran las vías pruritogénicas y promueven la colonización con Staphylococcus aureus, que es común en personas con EA.40-53
El profesor Leung agregó que la composición lipídica del estrato córneo es altamente anormal en las lesiones de EA. Por ejemplo, un cambio a lípidos de cadena corta en las lesiones de la EA permite que más agua se mueva a través del estrato córneo. El bloqueo de la señalización de IL-4 e IL-13 con dupilumab restaura la composición lipídica del estrato córneo y la función de barrera cutánea en pacientes con EA moderada a grave.42 En particular, el bloqueo de la señalización de IL-4 e IL-13 produjo un aumento progresivo de los lípidos de cadena larga en el estrato córneo y una mejor pérdida de agua transepidérmica (TEWL) en comparación con la línea de base, lo que indica una función cutánea normalizada. La mejora surgió ya en el día 15. En la semana 16, ninguno de los parámetros fue significativamente diferente en la piel lesionada en comparación con la piel sana, lo que indica la normalización de la piel atópica.54 La inflamación tipo 2 desregulada también impulsa la picazón crónica (ver más abajo).41 Los pruritogenos exógenos (como los alérgenos y las proteasas liberadas por S. aureus) y la barrera cutánea de disfunción desencadenan una respuesta de estrés epitelial. Como resultado, los queratinocitos liberan alarminas ('señales de peligro'), incluyendo linfopoyetina del estroma tímico, IL-25 e IL-33, que activan las células inmunes tipo 2 y estimulan la producción de citoquinas Th2, promoviendo la inflamación y los cambios en la integridad de la barrera cutánea.41 Además, varios pruritogénicos pueden activar los receptores activados por proteasa (PAR)-2 en las neuronas sensoriales.41 En otras palabras, el eje tipo 2 conduce a una diafonía neuroinmune-epitelial mejorada entre queratinocitos, células inmunes tipo 2, fibroblastos y pruriceptores (receptores de picazón) en la piel, lo que induce y amplifica la picazón.41
La inflamación tipo 2 actúa sobre una variedad de componentes de la barrera cutánea para impulsar la EA.
Muchos componentes estructurales y funcionales de la barrera epidérmica están desregulados en personas con EA, señaló la profesora Anna De Benedetto, profesora asociada de dermatología del Centro Médico de la Universidad de Rochester, Rochester, NY, EE. Explicó que la inflamación tipo 2 impulsa esta desregulación al influir en varios componentes esenciales para la estructura y función normal de la piel. Por ejemplo, la inflamación tipo 2 mejora la actividad de las proteasas, altera la expresión de varias proteínas estructurales (por ejemplo, filagrina, loricrina e involucrina) y aumenta los niveles de queratina 16. Las células sanas de la piel no expresan queratina 16, que es parte de una respuesta que regula las señales de peligro, la inmunidad innata y la función de barrera en la epidermis.40,55,56
En la piel sana, los lípidos repelentes al agua limitan la pérdida de agua y la penetración de alérgenos y patógenos. El profesor De Benedetto dijo que la inflamación tipo 2 produce un metabolismo, función y estructura de lípidos marcadamente disfuncionales en las lesiones de la EA.40 Por ejemplo, Elongases 3 y 6 (ELOVL3 y ELOVL6) estimulan la elongación de ácidos grasos. IL-4 e IL-13 inhiben la expresión de ELOVL3 y ELOVL6. Los pacientes con EA muestran una disminución de la expresión de ELOVL3 y ELOVL6. Como resultado, las ceramidas en el estrato córneo de las lesiones de EA tienen una longitud de cadena reducida, lo que contribuye a la disminución de la hidrofobicidad.57
En la piel sana, las uniones estrechas sellan los espacios entre las células. Esto forma la principal barrera para la difusión paracelular de fluidos, electrolitos, macromoléculas y patógenos.40 En las lesiones de EA, las uniones estrechas se vuelven permeables, lo que afecta la función de barrera epidérmica.40 Las citocinas, incluidas las características de la inflamación tipo 2, debilitan las uniones estrechas en las lesiones de EA.40 Esto tiene varias consecuencias, incluyendo:40,58-65
Función de barrera deteriorada.
Cambios en la posición y densidad del nervio sensorial (p. ej., las dendritas neurales penetran en la epidermis de las lesiones de la EA).
Retención de agua alterada.
Mayor susceptibilidad a la infección viral (incluyendo eczema herpeticum).
Las dendritas de las células de Langerhans (un tipo de célula presentadora de antígeno) alcanzan la superficie de la piel de la EA y capturan alérgenos. Por lo general, las células de Langerhans permanecen en las capas inferiores de la piel.
Además, las uniones estrechas claudina-1 y -3 evitan la fuga de sudor. En la EA, la pérdida de claudina-1 y -3 conduce a la fuga de sudor patógena.40,66 La inflamación tipo 2 socava la barrera formada por uniones estrechas y el estrato córneo que conduce a la fuga de sudor dentro de la epidermis. A su vez, la fuga de sudor resulta en: sequedad de la piel; retención de calor y reducción de la sudoración; mayor susceptibilidad a las infecciones; edema y picazón.40,63,66-68
El profesor De Benedetto agregó que la piel no lesional muestra una desregulación estructural y funcional similar a la de las lesiones de EA.69-71 De hecho, el aumento de la gravedad de la EA se correlaciona con una mayor interrupción de la barrera en la piel no lesionada en adultos y niños.69,70 Las comorbilidades atópicas pueden exacerbar la disfunción en la piel no lesional de las personas con EA. La alergia alimentaria, por ejemplo, se asocia con mayores alteraciones de la barrera cutánea no lesional en pacientes pediátricos con EA que en aquellos con piel sana.71 Los niños con sensibilización alérgica múltiple (cacahuete, huevo, gato o perro) muestran EA más grave y una mayor interrupción de la barrera cutánea que aquellos con EA y otras sensibilizaciones a alérgenos o piel sana.69
Disbiosis y EA
La colonización de la piel con S. aureus parece desarrollarse en una relación que se refuerza mutuamente con los otros procesos patógenos que subyacen a la EA. Por ejemplo, los pacientes con EA colonizada con S. aureus en su piel tienden a tener una enfermedad más grave, ejemplificada por una mayor disfunción de barrera, que aquellos que no albergan esta bacteria.72 Las toxinas, enzimas y otras proteínas liberadas por S. aureus, la causa más frecuente de brotes de EA inducidos por infección, pueden desencadenar la producción de alarmina por los queratinocitos, activar los mastocitos, interrumpir la barrera epidérmica y estimular las respuestas inmunes innatas y tipo 2.40,73,74
Entre el 30% y el 100% de los pacientes con EA están colonizados con S. aureus en comparación con el 5-30% de los controles sanos.73-75 S. aureus puede adherirse a la fibronectina y al fibrinógeno.40 En las lesiones de EA, se observa tinción de fibronectina en los estratos superiores de la epidermis, particularmente en el estrato córneo. La piel sana no muestra este patrón.75 La citoquina tipo 2 IL-4 aumenta la síntesis de procolágeno tipo I secretado y fibronectina entre dos y tres veces.76 La inflamación tipo 2 también promueve la colonización de S. aureus al reducir los niveles de péptidos antimicrobianos y aumentar el pH de la piel.40 Además, los receptores MSCRAMM (Microbial Surface Components Recognizing Adhesive Matrix Molecules) en la superficie de S. aureus se unen a proteínas de la matriz extracelular expresadas en la piel.75
Tomados en conjunto, estos hallazgos sugieren que la inflamación tipo 2 puede fomentar la colonización de S. aureus. La disbiosis resultante parece tener un papel central en la patogénesis de la EA. El profesor De Benedetto comentó, sin embargo, que se necesita más investigación para determinar si inicialmente S. aureus desencadena la EA o si los cambios en la estructura de la piel preceden a la colonización.
El eje neuroinmune y el mecanismo neuroinflamatorio del prurito
Gil Yosipovitch, profesor de dermatología de la Facultad de Medicina Miller de la Universidad de Miami y director del Miami Itch Center, Florida, EE.UU., señaló que la sensibilización neural es común en la EA. De hecho, la sensibilización neural impulsa la picazón, el dolor, la sensación de ardor y la piel sensible que suelen experimentar las personas con Alzheimer.79,80
El profesor Yosipovitch explicó que la inflamación tipo 2 contribuye a la sensibilización periférica y central (por ejemplo, reorganización cortical) y neuronal.79,80 En la piel de las personas con EA, los mediadores inflamatorios (p. ej., factor de crecimiento nervioso, prostaglandina E2 y artemina), la inervación anormal inducida por inflamación y rascado, y la activación de PAR-2 pueden inducir la sensibilización neural periférica.80
El profesor Yosipovitch enfatizó que la sensibilización neural no se limita a la periferia. La regulación positiva de los receptores y moléculas relacionados con el picor (por ejemplo, la sustancia P y el factor neurotrófico derivado del cerebro) en los ganglios de la raíz dorsal, la disfunción de los circuitos inhibitorios espinales y la atenuación de las vías inhibitorias descendentes contribuyen a la sensibilización neural central.80 La picazón prolongada también produjo cambios funcionales y estructurales en la corteza prefrontal y la corteza cingulada anterior.80 Juntos, estos cambios dan como resultado la sensibilización neuronal central.
Diafonía neuronal y del sistema inmunitario
Existe una considerable diafonía entre los sistemas neural e inmunológico, que tienen una relación muy dinámica, comentó el profesor Yosipovitch. La activación de las células inmunes y la liberación de citoquinas tipo 2 y otros mediadores inflamatorios estimulan y mejoran directamente la función neuronal en los sitios de inflamación.81-84 Por ejemplo, varios neuropéptidos (por ejemplo, péptido relacionado con el gen de la calcitonina, sustancia P y péptido intestinal vasoactivo) liberados por neuronas sensoriales desreguladas actúan directamente sobre las células inmunes, incluidos los eosinófilos, las células dendríticas, las células linfoides innatas, los mastocitos, los macrófagos y las células T.81,82,84 La vía de citoquinas tipo 2 y las integrinas también median la inducción de picazón e inflamación por periostina, una proteína de la matriz extracelular.85,86
Las citoquinas tipo 2 y otros mediadores que impulsan la actividad neuronal se originan a partir de interacciones complejas y dinámicas entre queratinocitos, células inflamatorias y terminaciones nerviosas, cascadas inmunes reguladas al alza, función de barrera epidérmica alterada y posible penetración de alérgenos en la piel.80 Varios factores modulan el impacto de estas interacciones, incluido el gradiente de pH, la integridad de la barrera cutánea, la exposición a irritantes y alérgenos, el microbioma (la colonización por S. aureus contribuye directamente a la neuroinflamación en la EA) y la neurosensibilización.80 87
El papel de los mastocitos
En ausencia de desencadenantes alérgicos, la expresión de la sustancia P en las fibras nerviosas y la expresión de triptasa aumentan en las lesiones de la EA. Al inicio del estudio, las lesiones de EA también muestran una mayor densidad de mastocitos, particularmente en la pidermis, y distancias más cortas entre los mastocitos y los nervios sensoriales en comparación con los controles.87 Además, los desencadenantes exógenos pueden activar el receptor acoplado a proteína G relacionado con Mas-X2 (MRGPRX2), un receptor que activa los mastocitos y es un importante impulsor de la picazón en la EA.87,88 La toxina δ de S. aureus puede activar directamente los mastocitos al unirse a MRGPRX2. Los microbios pueden impulsar la producción de péptido de defensa del huésped, que también activa MRGPRX2.87
A su vez, los mastocitos activados liberan histamina, que puede contribuir a la picazón. El profesor Yosipovitch señaló, sin embargo, que los antihistamínicos H2 convencionales son en gran medida ineficaces en la EA, lo que subraya el papel de las vías independientes de la histamina. De hecho, varias otras moléculas mediadoras de picazón (como IL-31, proteasas, péptidos y otros mediadores) se unen a los receptores en los pruriceptores, activando la vía independiente de la histamina.89,90 Las citoquinas tipo 2 también regulan al alza la vía independiente de la histamina.91
De hecho, la vía no histaminérgica es la principal responsable de la picazón crónica experimentada por las personas con EA, lo que explica la escasa eficacia de los antihistamínicos convencionales.91 El profesor Yosipovitch argumentó que los basófilos son la célula efectora clave asociada con el brote agudo de picazón en la EA desencadenada por IgE específica del alérgeno.92 Los basófilos activados por IgE también producen grandes cantidades de IL-4.93 La activación de basófilos puede ayudar a explicar los brotes de picazón experimentados por las personas con EA, sugirió el profesor Yosipovitch.
Métodos innovadores para evaluar la función de barrera de la piel
El profesor Cork presentó un video desarrollado como parte del programa educativo ADVENT que explora cómo los métodos innovadores para evaluar la función de barrera de la piel ofrecen información sobre la fisiopatología de la EA y el efecto de los tratamientos nuevos y existentes.
Una sonda en la piel mide de forma no invasiva TEWL al detectar cambios en la densidad del vapor de agua. Las directrices han ayudado a estandarizar la medición de TEWL. Trazar TEWL contra el número de tiras de cinta adhesiva permite calcular el área bajo la curva (TEWL AUC), que refleja la integridad del estrato córneo. Un AUC alto de TEWL refleja una mala integridad del estrato córneo. Un AUC TEWL bajo refleja una buena integridad. La medición del AUC de TEWL puede ofrecer una mejor evaluación de la integridad del estrato córneo que el TEWL basal solo. La extracción con cinta adhesiva cutánea es mínimamente invasiva y proporciona muestras para la evaluación de microbiómica, lipidómica, proteómica y transcriptómica.
Biopsias virtuales de piel
La tomografía de coherencia óptica (OCT) y la espectroscopia infrarroja por transformada de Fourier (FTIR) ofrecen una "biopsia virtual de piel" que permite evaluar la estructura de barrera. OCT proporciona una visualización tridimensional (3D) de la epidermis y la dermis papilar superior en resolución a escala micrométrica hasta 2 mm por debajo de la superficie.
La espectroscopia FTIR y Raman analiza de forma no invasiva la composición química de la piel para proporcionar una huella molecular del estrato córneo que muestra información estructural sobre la barrera cutánea in vivo. Las dos técnicas difieren en los métodos utilizados para crear una biopsia de piel virtual. La espectroscopia FTIR mide cuánta luz queda de la fuente original. La espectroscopia Raman mide la energía que se dispersa después de ser excitada por un láser.
Un espectrómetro FTIR portátil puede detectar la función de barrera de los pacientes con EA en la clínica. Esto permite la cuantificación instantánea de los factores hidratantes naturales (NMF) y el efecto del tratamiento. La espectroscopia FTIR y Raman también cuantifican la composición lipídica estructural del estrato córneo, el contenido de agua y los niveles de NMF. La combinación de la espectroscopia FTIR o Raman con la extracción de cinta adhesiva permite el análisis de toda la profundidad de la piel.
Fotografía 2D y 3D
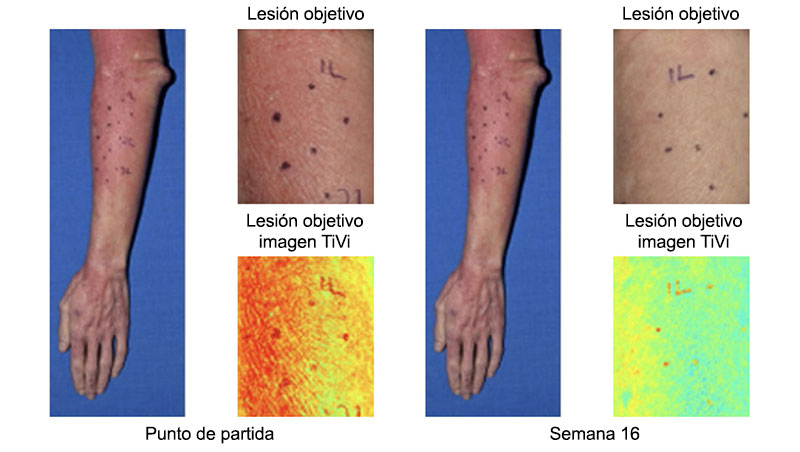
La fotografía bidimensional (2D) y 3D proporciona registros comparativos de la superficie de la piel que pueden ayudar a identificar cambios estructurales y funcionales en la función de barrera, así como a rastrear las mejoras clínicas. La fotografía tridimensional proporciona mayor detalle que las imágenes 2D, pero ambas ofrecen un registro altamente representativo de la mejora de la piel, especialmente desde la perspectiva del paciente.
Los filtros permiten el análisis de características como el volumen, el eritema y la pigmentación. Esto permite a los médicos utilizar el índice de viabilidad tisular. Los tonos amarillos y rojos representan una alta concentración de eritrocitos, que se asocia con un aumento del eritema. Los tonos azules y verdes representan una baja concentración de eritrocitos, que se asocia con una disminución del eritema.
El video educativo ilustra que los métodos en evolución para evaluar la función de barrera de la piel proporcionan nuevos conocimientos sobre la patología de la EA y cómo estos mecanismos subyacentes responden a los tratamientos existentes y de investigación. El uso de estos métodos en estudios clínicos mejorará la evaluación de los efectos de los tratamientos sobre la función de barrera cutánea en personas con EA en comparación con controles sanos. Los profesionales de la salud pueden ver el video en el Programa ADVENT | Educación médica para médicos sobre enfermedades inflamatorias tipo 2 | Dermatitis atópica y asma.
"Trabajar desde dentro": La normalización de la barrera cutánea como objetivo terapéutico
Los emolientes, los inmunosupresores tópicos (por ejemplo, TCS y tacrolimus), la ciclosporina y el dupilumab mejoran el TEWL basal de la piel lesionada en pacientes con EA moderada a grave, señaló el profesor Cork.94-96 Por ejemplo, durante la extracción secuencial de la piel, TEWL aumentó constantemente a una tasa reducida en sitios tratados con un emoliente que contiene urea, ceramida NP y lactato, lo que indica una mayor integridad del estrato córneo con el tiempo.94
Sin embargo, el profesor Cork señaló que el uso excesivo de TCS puede dañar la función de barrera.95 TEWL durante la extracción con cinta aumentó a una tasa significativamente menor con tacrolimus en comparación con la piel no tratada (p<0,0001) y la crema de valerato de betametasona (p<0,01).95 Además, un estudio comparó los cambios en TEWL con tres tratamientos. Los cambios en TEWL con TCS (-10.43 g/m2/h; p=0,047), ciclosporina (-7,73 g/m2/h; p=0,089) y dupilumab (-18,93 g/m2/h; p<0,001) sugirió mejoras en la función de barrera de la piel lesionada con EA. Sin embargo, en la piel no lesional, TEWL mejoró significativamente solo en pacientes que recibieron dupilumab (-3,62 g/m2/h; p=0,006).96
Un estudio retrospectivo investigó el efecto de dupilumab sobre la inflamación y la barrera epidérmica utilizando técnicas de inmunofluorescencia en pacientes con EA grave. El bloqueo de la señalización de IL-4 e IL-13 con dupilumab (n = 34; 300 mg cada 2 semanas después de una dosis de carga de 600 mg) normalizó los niveles de proteína estructural medidos mediante OCT. Después de 6-8 semanas de tratamiento con dupilumab, la OCT mostró aumentos estadísticamente significativos en la expresión de filagrina (p<0,01), inhibidor linfoepitelial relacionado con Kazal (un inhibidor de la proteasa; p<0,01) y beta-defensina-3 humana (un péptido antimicrobiano; p<0,001).97 En otro estudio, los pacientes con EA moderada a grave fueron aleatorizados para recibir dupilumab 200 mg semanales o placebo (ambos n = 27). Después de 16 semanas, dupilumab disminuyó la hiperplasia epidérmica y el engrosamiento (basado en la tinción de queratina 16) y aumentó los niveles de filagrina.98
El estudio BALISTAD
En este contexto, el estudio Dupilumab Skin Barrier Function Study in Atopic Dermatitis (BALISTAD) incluyó a 26 pacientes con EA de entre 12 y 65 años con EA moderada a grave, que eran elegibles para dupilumab y 26 controles sanos emparejados por edad, sexo, ubicación corporal y sitio de estudio. Los pacientes recibieron una dosis de carga de dupilumab (600/400 mg) el día 1, seguida de 300/200 mg cada 2 semanas hasta la semana 14.99
Al inicio del estudio, la TEWL fue significativamente diferente entre la piel sana y la piel lesionada y no lesional. En la semana 16, el bloqueo de la señalización de IL-4 e IL-13 normalizó la función de barrera medida por TEWL después de cinco tiras de cinta adhesiva cutánea en piel lesional (p = 0.225 vs controles) y no lesional (p = 0.163). De hecho, el bloqueo de la señalización de IL-4 e IL-13 se asoció con un aumento progresivo de los lípidos de cadena larga en el estrato córneo que fue significativo ya en el día 15 (Figura 8). Esto confirma una correlación entre la mejora de los lípidos y la normalización de la función de barrera. Los resultados clínicos e informados por los pacientes también mejoraron en la semana 16.99
Resolución de la disbiosis
El bloqueo de IL-13 con tralokinumab se asoció con una reducción 10 veces mayor desde el inicio en la abundancia de S. aureus (p<0.0001) y una mayor diversidad microbiana (p<0.001) en las lesiones de AD después de la semana 16.100 El bloqueo de la señalización de IL-4 e IL-13 con dupilumab (200 mg una vez a la semana) también redujo la abundancia de S. aureus en la piel y aumentó significativamente la diversidad del microbioma en comparación con placebo (p<0.001) durante 16 semanas de tratamiento.101
En un reciente estudio aleatorizado doble ciego, los pacientes recibieron 6 semanas de tratamiento con dupilumab seguido de una fase abierta de 10 semanas. La abundancia de S. aureus (cuantificada mediante reacción en cadena de la polimerasa) mostró una marcada reducción de la piel lesional de la EA ya en el día 3 (p = 0,02), que se hizo más significativa después de al menos 14 días de seguimiento (p<0,001). Las reducciones significativas en la abundancia de S. aureus cuantificadas mediante cultivo también surgieron ya en el día 3 (p<0,001) en las lesiones de la EA.102 La piel no lesional mostró una abundancia reducida a los 21 días (p<0,001).102 El profesor Cork explicó que la normalización de la piel lesional parece reducir la adhesión de S. aureus, como se discutió anteriormente.40,76
El profesor Cork concluyó que dirigirse a la inflamación tipo 2, en particular IL-4 e IL-13, con productos biológicos puede mejorar significativamente la barrera epidérmica y normalizar la función de barrera cutánea en pacientes con EA moderada a grave.94,96,98-100,102 La "normalización" de los mecanismos moleculares desregulados en la EA al dirigirse a la inflamación tipo 2 puede restaurar la barrera cutánea y normalizar la función de barrera, lo que se refleja en mejoras en los signos clínicos, los síntomas y la CdV de los pacientes.54,99
ADVENT.
Estos simposios son parte de ADVENT, un programa de educación médica no promocional para profesionales de la salud, organizado por Sanofi y Regeneron Pharmaceuticals, para avanzar en la comprensión de la inflamación tipo 2. ADVENT, una colaboración con más de 50 expertos globales, vincula la ciencia más reciente de la inflamación tipo 2 con el manejo clínico para mejorar la atención al paciente. Puede acceder al programa en: www.adventprogram.com.
Referencias.
Silverberg JI et al. Ann Allergy Asthma Immunol 2021;126:417–428.e2
Barbarot S et al. J Pediatr 2022;246:220–226.e5
Cork MJ et al. J Dermatolog Treat 2020;31:801–809
Paller A et al. Presentado en ESPD 2022; Reunión híbrida; 20 y 22 de mayo de 2022
de Carvalho V et al. Presentado en RAD 2022; 9 – 12 abril. Cartel 211
Weidinger S et al. Presentado en la reunión del DEUC, 20 y 22 de mayo de 2022
Silverberg J et al. Presentado en el SPD; Del 8 al 10 de julio de 2021
Gandhi NA et al. Nat Rev Drug Discov 2016;15:35–50
Baiardini I et al. Presentado en el congreso EADV; 7 al 10 de septiembre de 2022
Shah S et al. Póster presentado en la Reunión Anual de SID. 18–21 de mayo de 2022
Galli E et al. Presentado en el congreso EADV; 7 al 10 de septiembre de 2022
de Bruin-Weller M et al. Presentado en el congreso EADV; 7 al 10 de septiembre de 2022
Hanifin JM et al. Exp Dermatol 2001;10:11-8
Charman CR et al. Arch Dermatol 2004;140:1513-9
Lewis-Jones MS, Finlay AY. Br J Dermatol 1995;132:942-9
Lewis-Jones MS et al. Br J Dermatol 2001;144:104-10
Howells LM et al. Br J Dermatol 2020;183:524-536
Ramírez FD et al. JAMA Pediatr 2019;173:e190025
Neri I et al. Presentado en EADV; 7 al 10 de septiembre de 2022
Silverberg J et al. Presentado en EADV; 7 al 10 de septiembre de 2022
Huang AH et al. J Am Acad Dermatol 2021;85:893–900
Ong PY, Leung DY. Immunol Allergy Clin North Am 2010;30:309–321
Paller A et al. Presentado en AAD 2022; 25–29 de marzo
Weidinger S et al. Presentado en la conferencia virtual del SPD; 8–10 de julio de 2021
Pálsson K et al. J Eur Acad Dermatol Venereol 2021;35:1849–1858
Hou A, Silverberg JI. Pediatr Dermatol 2021;38:606–612
Kern C et al. JAMA Dermatol 2021; 157:1200–1208
Stingeni L et al. J Alergia al asma 2021;14:919–928
Paller AS et al. J Am Acad Dermatol 2022;DOI:10.1016/j.jaad.2022.01.018
Paller AS et al. BMJ Abierto 2020;10:e033507
Paller AS et al. Presentado en EADV; 7 al 10 de septiembre de 2022
Sidbury R et al. J Am Acad Dermatol 2014;71:327–349
Paller AS et al. Medicamentos pediátricos 2021;23:515–527
Paller AS et al. J Am Acad Dermatol 2020;83:1282–1293
Cork MJ et al. Br J Dermatol 2021;184:857–870
Wollenberg A et al. Acta Derm Venereol 2022;102:adv00726
Paller AS et al. Presentado en el Congreso Digital AAD 2021; 23 y 25 de abril
Irvine A et al. Presentado en el Congreso Digital de AAD; 23 y 25 de abril de 2021. P27431
Haddad EB et al. Dermatol Ther (Heidelb) 2022;12:1501-1533
Beck LA et al. JID Innovations 2022;2:DOI:10.1016/j.xjidi.2022.100131
Garcovich S et al. Vacunas 2021;9:303
Allen JE, Sutherland TE. Semin Immunol 2014;26:329-40
Makepeace BL et al. Curr Med Chem 2012;19:1567-86
Inclan-Rico JM, Siracusa MC. Tendencias Parasitol 2018;34:861-880
de Kouchkovsky DA et al. Tendencias Immunol 2017;38:154-167
Weatherhead JE et al. Frente Immunol 2020;11:594520
Noda S et al. J Alergia Clin Immunol 2015;136:1254–1264
Sanyal RD et al. Ann Allergy Asthma Immunol 2019;122:99–110.e6
Brunner PM, Guttman-Yassky E. Ann Alergia Asma Immunol 2019;122:449–455
Brunner PM et al. J Alergia Clin Immunol 2018;141:2094–2106
Esaki H et al. J Allergy Clin Immunol 2016;138:1639–1651
Brunner PM et al. Ann Allergy Asthma Immunol 2019;122:318–330.e3
Farag AK et al. Alergia 2022;77:1245–1253
Berdyshev E et al. Alergia DOI:10.1111/ all.15432
Suárez-Fariñas M et al. J Allergy Clin Immunol 2011;127:954–64.e1–4
Lessard JC et al. Proc Natl Acad Sci USA 2013;110:19537–19542
Berdyshev E et al. JCI Insight 2018;3:DOI:10.1172/jci.insight.98006
Bergmann S et al. Sci Rep 2020;10:2024
Furuse M et al. J Cell Biol 2002;156:1099–1111
Sugawara T et al. J Derm Sci 2013;70:12–18
Nadeau P et al. J Alergia Clin Immunol 2018;142:281–284.e7
De Benedetto A et al. J Allergy Clin Immunol 2011;128:242–246.e5
De Benedetto A et al. J Clin Med 2015;4:741–55
Gruber R et al. Am J Pathol 2015;185:2777–2789
Takahashi S et al. Sci Rep 2019;9:8625
Yamaga K et al. J Invest Dermatol 2018;138:1279–1287
Hönzke S et al. J Invest Dermatol 2016;136:631–639
Yokouchi M et al. J Dermatol Sci 2015;77:28–36
Sherenian MG et al. Clin Exp Allergy 2021;51:666–673
Yoshida T et al. Allergol Int 2022;71:3–13
Leung DYM et al. Sci Transl Med 2019;11:eaav2685
Simpson EL et al. J Invest Dermatol 2018;138:2224–2233
Kim J et al. Alergia Asma Immunol Res 2019;11:593–603
Paller AS et al. J Allergy Clin Immunol 2019;143:26–35
Cho SH et al. J Allergy Clin Immunol 2001;108:269–74
Postlethwaite AE et al. J Clin Investig 1992;90:1479–1485
Nedoszytko B y otros Int J Mole Sci 2020;21:6484
Serezani APM et al. J Allergy Clin Immunol 2017;139:142–151.e5
Baliki MN, Apkarian AV. Neuron 2015;87:474–491
Yosipovitch G et al. Acta Derm Venereol 2019;99:1201–1209
Kabata H, Artis D. J Clin Invest 2019;129:1475–1482
Mack MR, Kim BS. Trends Immunol 2018;39:980–991
Zeidler C, Ständer S. Eur J Pain 2016;20:37–40
Ohanyan T et al. Acta Derm Venereol 2018;98:26–31
Ono J et al. Biomoléculas 2021;11:1084
Hashimoto T et al. J Invest Dermatol 2021;141:2338–2343
Wang Z, Babina M. Exp Dermatol 2020;29:1104–1111
Navinés-Ferrer A et al. Sci Rep 2018;8:11628
Paller AS et al. J Alergia Clin Immunol 2017;140:633–643
Kühn H et al. J Alergia Clin Immunol 2021;147:456–469
Yang TB, Kim BS. J Alergia Clin Immunol 2019;144:353–360
Wang F et al. Celda 2021;184:422–440.e17
Brunner T et al. J Exp Med 1993;177:605–11
Danby SG et al. Skin Pharmacol Physiol 2016;29:135–47
Chittock J et al. Acta Derm Venereol 2015;95:653–8
Montero-Vilchez T et al. J Clin Med 2022;11:DOI:10.3390/jcm11123341
Rohner MH et al. Alergia 2021;76:1268–1270
Guttman-Yassky E et al. J Alergia Clin Immunol 2019;143:155–172
Bissonnette R et al. Presentado en la Conferencia RAD; 11 y 13 de diciembre de 2021
Bieber T et al. Presentado en AAD VMX; 23-25 de abril de 2021; ID del póster: 28170
Callewaert C et al. J Invest Dermatol 2020;140:191–202.e7
Beck LA. Presentado en AAAI. 25 y 28 de febrero de 2022. Presentación 2521

Recomendamos